Практическая работа. Осуществление цепочки химических превращений ГЛАВА 2. Свойства металлов и их соединений химический практикум. Осуществление цепочки химических превращений. Получение и свойства соединений металлов. Цель провести. Общие химические свойства металлов взаимодействие с неметаллами, водой. Adamyn/image186.jpg' alt='Цепочки Превращений Металлы' title='Цепочки Превращений Металлы' />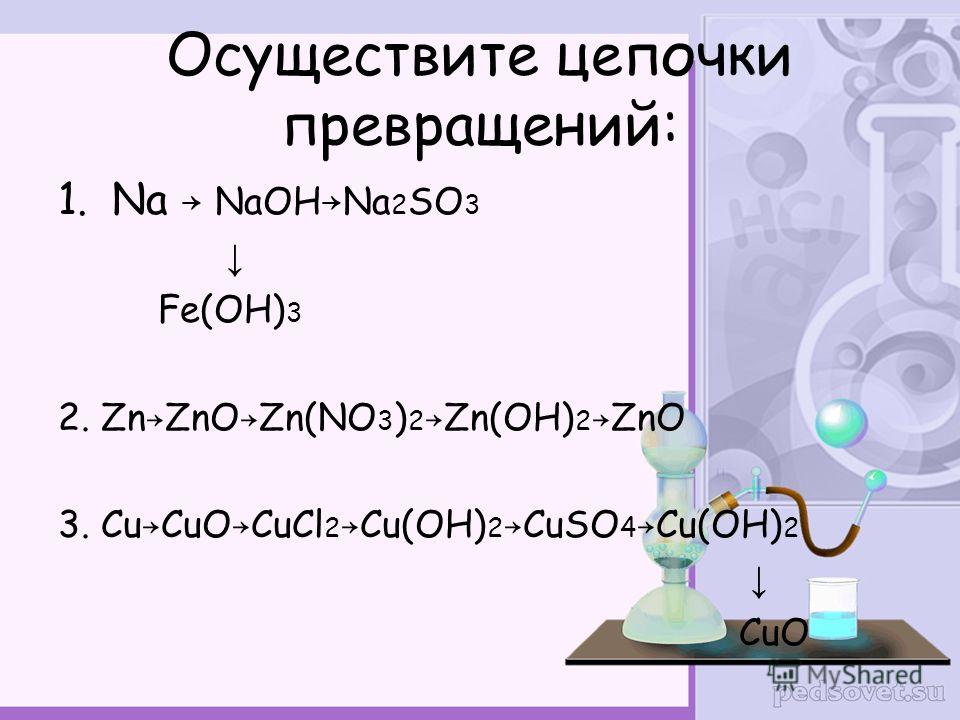 Разбор принципов решения цепочек превращения по химии на примерах Ссылки на плейлисты с цепочками превращений 1 Цепочки. Щелочные металлы относятся к sэлементам и имеют один валентный электрон на внешнем уровне ns1. Сверху вниз в. Цепочки превращений. Варианты заданий ЕГЭ по химии часть С1,С2 цепочки превращений, задачи на примере щелочных металлов и их соединений. Решение цепочек превращений по химии. Осуществить цепочку превращений. Дать названия. Контрольная работа по химии для 9 класса по теме Металлы. Контрольная. Кроме того, реакции и цепочки превращений, относящиеся к. Учебно методический материал химия, 9 класс по теме Инструкции для практических работ по химии к учебнику О. С. Кировск Румянцева Е. М. 2. 01. 3Практическая работа. Инструкция к выполнению первой цепочки переходов. Выданы пробирки. Для осуществления превращений приливайте по 1 2 мл необходимых реактивов после проведения 1 ого опыта отделите раствор от непрореагировавшего вещества, слейте его в пр. Инструкция к выполнению второй цепочки переходов. Для осуществления второй цепочки переходов выданы пробирки. Для отчта оформите таблицу Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Для осуществления 1 ого опыта приливайте 1 2 мл необходимого реактива. Второй и третий переход проводите в этой же пробирке. В пробирку. В обе пробирки прилейте по 1 2 мл раствора хлорида алюминия и получите в обеих пробирках студенистый осадок гидроксида алюминия используйте 1 2 мл раствора реактива. Вы должны услышать либо глухой хлопок п пах, либо лающий звук в чм причина различий. Заполните таблицу, напишите уравнения 2 ух проведнных реакций, составьте электронный баланс, сделайте выводы о лабораторном способе получения, собирания и распознавания водород. Оформите отчт в таблице. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Не прекращая нагревания, определите наличие аммиака по изменению цвета влажной фенолфталеиновой бумажки, поднеснной к отверстию пробирки примника. Опустите пробирку с аммиаком в кристаллизатор с водой, впустите капельку воды, закройте снова пробирку под водой, палец будет втягиваться в пробирку, так как в ней образовался вакуум. Снова под водой отнимите палец. Что наблюдаете 5Закройте пробирку пальцем под водой и выньте е из сосуда. Разделите содержимое пробирки на две части В одну добавьте 2 3 капли фенолфталеина, в другую 2 3 капли хлорида алюминия. Составьте отчт, заполнив таблицу, составьте 3 уравнения проведнных реакций, сделайте вывод о лабораторном способе получения, собирания и распознавания аммиака. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности 1Соберите прибор Кирюшкина для получения газа, проверьте его на герметичность. В пробирку на резиновое кольцо поместите несколько кусочков мрамора. Откройте зажим и прилейте в воронку соляной кислоты так, чтобы она покрыла поверхность мрамора. Опускайте газоотводную трубку поочердно в пробирки По окончании опыта закройте зажим. Заполните таблицу см. Опыт. 2 получение, собирание и распознавание кислорода. Соберите прибор для получения газа наденьте на пробирку. Что наблюдаете Закройте сразу пробирку пробкой с газоотводной трубкой. Поместите газоотводную трубку в пустой химический стакан через некоторое время проверьте наличие в нм кислорода тлеющей лучинкой. Составьте отчт, заполнив таблицу Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт. 1. Повторите правила техники безопасности Выполняем задания из учебника. Необходимо определить в какой из трх пробирок находится раствор соляной кислота, в какой серной кислоты, в какой гидроксида натрия. Прилейте 3 4 мл дистиллированной воды, растворите соль, разделите раствор соли на две пробирки часть отлейте в пр. Повторите правила техники безопасности Выполняем задания из учебника. Прилейте в не 2 3 мл серной кислоты. Что наблюдаете Составьте уравнение методом электронного баланса, укажите окислитель и восстановитель. В пробирках. Составьте молекулярные и ионные уравнения реакций. В пробирку. Для отчта оформите таблицу. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Определите в какой пробирке находится каждое из веществ с помощью одного реактива. Что наблюдаете Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. В пробирку. Добавьте 2 3 капли выбранного вами реактива для проведения реакции обмена к полученному осадку опишите его внешний вид, характер добавляйте реактив до получения алюмината натрия. Заполните таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. 8. 6 и задание. Определите, в какой пробирке находится каждое из веществ с помощью одного реактива а растворите каждое из исследуемых веществ в 3 4 мл воды б прилейте в пробирки. Что наблюдаете Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. В пробирке. Для того, чтобы определить, содержит ли он примесь сульфата железа III а растворите образец в 3 4 мл дистиллированной воды б добавьте 1 2мл раствора выбранного вами реактива. Заполните таблицу запишите уравнения проделанной реакции в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности Вариант. Получите гидроксид алюминия по реакции обмена согласно уравнению Al. Cl. 3 3. Na. ОН AlOH3 3. Na. Cl. Проверим, справедливо ли для химии математическое выражение от перемены мест слагаемых сумма не изменяется. Для этого проведм данную реакцию двумя способами а в пробирку. Что наблюдаете б в пробирку. Выпал ли осадок Составьте ионные уравнения проведнной реакции, объясните результаты опыта. Руководство По Ремонту Газ 31105 Змз 406. Оформите отчт в таблицу. Оформите отчт в таблицу. По заданию . 8. 5 учебника изменнное. Проведите реакции, подтверждающие качественный состав хлорида железа III а в пробирку. Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности Вариант. Определите, в какой пробирке находится каждое из веществ с помощью одного реактива а определите теоретически реактив б прилейте по несколько капель раствора выбранного вами реактива в каждую пробирку. Что наблюдаете Составьте молекулярные и ионные уравнения проделанных реакций. Отчт оформите в таблицу. Составьте отчт, заполнив таблицу. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы.
Разбор принципов решения цепочек превращения по химии на примерах Ссылки на плейлисты с цепочками превращений 1 Цепочки. Щелочные металлы относятся к sэлементам и имеют один валентный электрон на внешнем уровне ns1. Сверху вниз в. Цепочки превращений. Варианты заданий ЕГЭ по химии часть С1,С2 цепочки превращений, задачи на примере щелочных металлов и их соединений. Решение цепочек превращений по химии. Осуществить цепочку превращений. Дать названия. Контрольная работа по химии для 9 класса по теме Металлы. Контрольная. Кроме того, реакции и цепочки превращений, относящиеся к. Учебно методический материал химия, 9 класс по теме Инструкции для практических работ по химии к учебнику О. С. Кировск Румянцева Е. М. 2. 01. 3Практическая работа. Инструкция к выполнению первой цепочки переходов. Выданы пробирки. Для осуществления превращений приливайте по 1 2 мл необходимых реактивов после проведения 1 ого опыта отделите раствор от непрореагировавшего вещества, слейте его в пр. Инструкция к выполнению второй цепочки переходов. Для осуществления второй цепочки переходов выданы пробирки. Для отчта оформите таблицу Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Для осуществления 1 ого опыта приливайте 1 2 мл необходимого реактива. Второй и третий переход проводите в этой же пробирке. В пробирку. В обе пробирки прилейте по 1 2 мл раствора хлорида алюминия и получите в обеих пробирках студенистый осадок гидроксида алюминия используйте 1 2 мл раствора реактива. Вы должны услышать либо глухой хлопок п пах, либо лающий звук в чм причина различий. Заполните таблицу, напишите уравнения 2 ух проведнных реакций, составьте электронный баланс, сделайте выводы о лабораторном способе получения, собирания и распознавания водород. Оформите отчт в таблице. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Не прекращая нагревания, определите наличие аммиака по изменению цвета влажной фенолфталеиновой бумажки, поднеснной к отверстию пробирки примника. Опустите пробирку с аммиаком в кристаллизатор с водой, впустите капельку воды, закройте снова пробирку под водой, палец будет втягиваться в пробирку, так как в ней образовался вакуум. Снова под водой отнимите палец. Что наблюдаете 5Закройте пробирку пальцем под водой и выньте е из сосуда. Разделите содержимое пробирки на две части В одну добавьте 2 3 капли фенолфталеина, в другую 2 3 капли хлорида алюминия. Составьте отчт, заполнив таблицу, составьте 3 уравнения проведнных реакций, сделайте вывод о лабораторном способе получения, собирания и распознавания аммиака. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности 1Соберите прибор Кирюшкина для получения газа, проверьте его на герметичность. В пробирку на резиновое кольцо поместите несколько кусочков мрамора. Откройте зажим и прилейте в воронку соляной кислоты так, чтобы она покрыла поверхность мрамора. Опускайте газоотводную трубку поочердно в пробирки По окончании опыта закройте зажим. Заполните таблицу см. Опыт. 2 получение, собирание и распознавание кислорода. Соберите прибор для получения газа наденьте на пробирку. Что наблюдаете Закройте сразу пробирку пробкой с газоотводной трубкой. Поместите газоотводную трубку в пустой химический стакан через некоторое время проверьте наличие в нм кислорода тлеющей лучинкой. Составьте отчт, заполнив таблицу Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт. 1. Повторите правила техники безопасности Выполняем задания из учебника. Необходимо определить в какой из трх пробирок находится раствор соляной кислота, в какой серной кислоты, в какой гидроксида натрия. Прилейте 3 4 мл дистиллированной воды, растворите соль, разделите раствор соли на две пробирки часть отлейте в пр. Повторите правила техники безопасности Выполняем задания из учебника. Прилейте в не 2 3 мл серной кислоты. Что наблюдаете Составьте уравнение методом электронного баланса, укажите окислитель и восстановитель. В пробирках. Составьте молекулярные и ионные уравнения реакций. В пробирку. Для отчта оформите таблицу. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Определите в какой пробирке находится каждое из веществ с помощью одного реактива. Что наблюдаете Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. В пробирку. Добавьте 2 3 капли выбранного вами реактива для проведения реакции обмена к полученному осадку опишите его внешний вид, характер добавляйте реактив до получения алюмината натрия. Заполните таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. 8. 6 и задание. Определите, в какой пробирке находится каждое из веществ с помощью одного реактива а растворите каждое из исследуемых веществ в 3 4 мл воды б прилейте в пробирки. Что наблюдаете Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. В пробирке. Для того, чтобы определить, содержит ли он примесь сульфата железа III а растворите образец в 3 4 мл дистиллированной воды б добавьте 1 2мл раствора выбранного вами реактива. Заполните таблицу запишите уравнения проделанной реакции в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности Вариант. Получите гидроксид алюминия по реакции обмена согласно уравнению Al. Cl. 3 3. Na. ОН AlOH3 3. Na. Cl. Проверим, справедливо ли для химии математическое выражение от перемены мест слагаемых сумма не изменяется. Для этого проведм данную реакцию двумя способами а в пробирку. Что наблюдаете б в пробирку. Выпал ли осадок Составьте ионные уравнения проведнной реакции, объясните результаты опыта. Руководство По Ремонту Газ 31105 Змз 406. Оформите отчт в таблицу. Оформите отчт в таблицу. По заданию . 8. 5 учебника изменнное. Проведите реакции, подтверждающие качественный состав хлорида железа III а в пробирку. Составьте отчт, заполнив таблицу запишите уравнения проделанных реакций в молекулярном и ионном видах. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы. Опыт 1. Повторите правила техники безопасности Вариант. Определите, в какой пробирке находится каждое из веществ с помощью одного реактива а определите теоретически реактив б прилейте по несколько капель раствора выбранного вами реактива в каждую пробирку. Что наблюдаете Составьте молекулярные и ионные уравнения проделанных реакций. Отчт оформите в таблицу. Составьте отчт, заполнив таблицу. Ход работы. Наблюдение, Рисунок Уравнения реакций Выводы.
Навигация
- Комиксы Симпсоны Pdf
- Плюсы И Минусы Интернета Презентация
- Фильм Римская Империя
- Бланк Извещения Об Изменении Кд
- Критерии Mcdonald
- Учебник Технология Приготовления Мучных Кондитерских Изделий Бутейкис
- Фоллаут 3 Установочник
- Программу Для Автоматического Составления Графика Работ
- Миранда Гуссокл Книга Заклинаний
- Пупо Торрент
- Программа Sett Mett Mimika